武育蓉医生的科普号
- 精选 动脉导管未闭科普小课堂
1.什么是动脉导管未闭?宝宝在妈妈腹中时,动脉导管将肺动脉和主动脉相连,是胎儿血液循环的重要通道,保证胎儿降主动脉血液的供应。出生以后,当孩子应用自己的肺部呼吸后,动脉导管就会渐渐关闭,大部分孩子在出生后1周内关闭,80%的宝宝在3个月里都会关闭。超过3个月还没有关闭,就称为动脉导管未闭,就属于先天性心脏病了,是最常见的小儿先天性心脏病之一。早产儿的动脉导管未闭发生率比足月儿要高。2.动脉导管未闭的宝宝会有什么表现?宝宝的表现和动脉导管的粗细有关。导管细小的宝宝可以没有明显症状,只是在体检的时候听到心脏杂音,有些患儿甚至连心脏杂音都没有,只是因为其他原因做心脏超声检查时发现有动脉导管未闭。而导管比较粗大的宝宝常出现生长发育落后、体重增加慢、吃奶费力,还会变得更容易生病,反复感冒、肺炎。通过导管分流量大的宝宝会有心前区突出、鸡胸等表现。3.怎么检查动脉导管未闭?心脏超声是诊断动脉导管未闭最常用的方式,能够评估动脉导管的大小、长短和形态、分流的情况等,对于了解病情的严重程度和决定后续的治疗方式都十分有帮助。同时也对宝宝没有创伤,是非常安全的检查方式。当宝宝出现相关表现,或是体检时医生听到心脏杂音、怀疑动脉导管未闭时,都应该做心脏超声来明确诊断。4、当检查发现动脉导管未闭时,应该怎么办呢?患儿1岁以内,动脉导管未闭都有可能自然闭合,越是细小的动脉导管未闭,自然闭合的几率越高。所以在发现动脉导管未闭后,不一定需要立即治疗。要请小儿心脏科医师来进一步评估。一般来讲,比较细小的动脉导管未闭,没有明显的症状,不需要立即治疗。比较粗大的动脉导管未闭,可能影响孩子的生长发育,需要早期治疗。导管是否粗大或细小,要由专业的小儿心脏科医师根据患儿的症状来判断,不要只看具体的心脏超声中描述的动脉导管的数字。5、怎样治疗动脉导管未闭?当宝宝确认动脉导管不能自行闭合,或是粗大的动脉导管导致孩子出现明显的临床表现时,就需要进行治疗了。推荐在学龄前治疗完成,让宝宝能够健康地开始学习生活。具体的治疗方法有微创介入手术和外科开胸手术两种。1)微创介入手术:绝大部分动脉导管未闭的宝宝都可以通过微创介入的方法治疗。相对于外科开胸手术而言,介入治疗伤口小,只在大腿根部留下一个小小的伤口;恢复快,术后第二天即可下地走路,住院时间不到一周,术后也不需要再服用药物。不过,也会有一些宝宝不适合介入的治疗,需要医生在整体评估病情后给出最适合宝宝的个体化方案。2)外科开胸手术:早产儿的动脉导管未闭因为体重偏小,需要应用开胸手术的方式治疗。此外,少数非常大的动脉导管,或者导管形态特殊时,需要开胸手术治疗。目前即便是新生儿时期的开胸手术,技术也十分成熟,成功率非常高。6、动脉导管未闭治疗效果好吗?无论是通过微创介入的方法,还是外科开胸手术的方法治疗,动脉导管未闭通过及时的治疗后,预后都非常好,和正常人一模一样,对孩子的生长发育和未来生活没有影响。7、动脉导管未闭可以打预防针吗?细小的动脉导管未闭的宝宝是可以正常预防接种的。少数粗大的动脉导管,出现生长发育落后、体重增长欠佳等情况的宝宝应该暂缓预防针,在治疗、恢复后再补种。
武育蓉 主任医师 上海新华医院 儿童心脏中心 小儿心血管科22人已购买 - 精选 室间隔缺损科普小课堂
1.什么是室间隔缺损?我们的心脏有四个心腔,分别是右心房、左心房和右心室、左心室。左右心室之间有一间隔称室间隔,这个间隔有先天缺损即称为室间隔缺损。室间隔缺损是最常见的小儿先天性心脏病之一。2.室间隔缺损的宝宝有什么表现呢?室间隔缺损的宝宝会出现什么症状与室间隔缺损的大小有关。缺损较小时可无明显症状,仅检查时可以听到杂音,缺损大时,则会出现宝宝生长发育落后于同龄的小孩,体重增加不明显,宝宝会容易生病,反复出现肺炎,还会出现多汗,哭吵后嘴唇青紫的现象。3.检查室间隔缺损有哪些方式?室间隔缺损可以通过心脏超声诊断,同时心脏超声还可以对室间隔缺损的大小、部位、肺动脉压力、瓣膜情况等进行评估。若是宝宝体检时,医生怀疑有室间隔缺损,那么一定要做心脏超声明确诊断。4.宝宝有室间隔缺损怎么办?根据宝宝室间隔缺损的大小与部位的不同,可以选择不同的治疗方案。对于缺损小的宝宝,一般不会出现反复呼吸道感染、生长发育落后等表现,不需要早期治疗,可以定期复查和随访。膜周部和肌部室间隔缺损都有可能自然闭合。若缺损较大,孩子在2-3月龄时就会出现体重不增长、多汗、气急、哭吵后青紫、易激惹、反复肺炎等临床表现,如果出现这些症状,那么就说明孩子有心力衰竭和肺动脉高压的表现,需要早期治疗。4.室间隔缺损的治疗方式具体治疗的方式有两种:(1)微创介入手术:一般来说,介入治疗应用于中小型室间隔缺损,年龄大于2岁以上的宝宝。介入治疗相对于开胸手术来说,创伤小,只会在宝宝的大腿根部有一个小伤口,恢复快,看起来也更美观。但是室间隔缺损的介入治疗非常强调个体化方案,对于室间隔缺损的部位、和周边瓣膜的关系等都有要求,所以要根据每个宝宝的具体情况来制定方案,不是所有室间隔缺损都可以选择介入治疗的方式。(2)外科开胸手术:大部分室间隔缺损都可以通过开胸手术的方式治疗。开胸手术方式一般为胸骨正中切口,相对介入来说,开胸手术创伤较大,恢复时间长,一般需要住院2周左右。但是技术非常成熟,手术成功率非常高,也不必过分担心。5.室间隔缺损预后如何?对于室间隔缺损小的宝宝来说,有自然闭合的机率,缺损闭合后则与正常的宝宝一样。对于缺损较大的宝宝,需在小婴儿时行手术治疗,在治疗后可以完全治愈,和正常的宝宝是一样的。所以,室间隔缺损这种先天性心脏病的预后是非常好的。6.室间隔缺损的宝宝可以打预防针么?对于室间隔缺损大小5mm以上,有肺动脉高压、心衰的宝宝来说,不建议打预防针。小型的室间隔缺损是可以预防接种的。本文系武育蓉医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
武育蓉 主任医师 上海新华医院 儿童心脏中心 小儿心血管科78人已购买 - 精选 房间隔缺损科普小课堂
1.什么是房间隔缺损?通俗的讲,房间隔缺损是指在心脏的房间隔上存在一个孔,导致左心房和右心房之间相通。正常的心脏两个心房之间应该是不相通的,所以三个月以上的孩子如果房间隔上有孔导致两个心房相通,则认为是先天性心脏病。许多家长一听先天性心脏病这个名词就非常紧张,不是很有必要。房间隔缺损这种先天性心脏病是否会对孩子的健康造成影响,主要取决于缺损的大小,下面听我娓娓道来。2.宝宝有房间隔缺损会有什么症状呢?房间隔缺损是否会产生症状取决于缺损的大小,一般来说,4mm以下的房间隔缺损属于小型缺损。小型的房间隔缺损一般是没有明显的临床症状的,可能是在因为其他原因做心超检查时被偶尔发现的。中等大小或者较大的房间隔缺损临床上可能仅仅表现为心脏杂音,临床上很多房间隔缺损都是因为在体检时听到心脏杂音而进一步心脏超声检查后明确的。也可能表现为体质偏差容易感冒等。总得来讲,房间隔缺损一般不会出现其他先天性心脏病等常见的患儿生长发育落后或者青紫等的表现。3.房间隔缺损需要做什么检查呢?一般情况下,房间隔缺损应用心脏超声检查就可以确诊。少数情况下如果有其他合并畸形,可能需要进一步做心脏CT或者磁共振检查。4.宝宝有房间隔缺损可以自愈么?小型的房间隔缺损是有可能自愈的,而且自然闭合的几率还比较高,有报道出生一周的宝宝超声检查房间隔上有一孔洞的约占24%,一岁后约92%可以自闭。中大型的房间隔缺损自然闭合的几率较低,需要定期超声随访。5.房间隔缺损怎样治疗呢?小型的房间隔缺损,因为不会引起症状,对身体没有危害,所以一般不需要治疗,只需要定期超声随访就好。中等或大型房缺自行闭合的可能性不大,会引起心脏负荷过重而导致右心房右心室增大,严重的还可以引起肺动脉高压,所以需要治疗。治疗的方式有以下两种:(1)微创介入手术——如果患儿的房间隔缺损是中央型的,缺损距离周边的血管和瓣膜超过5mm以上,就可以考虑介入治疗。这种手术最大的优点是创伤小,比较美观,从住院到出院一般只需要1周的时间,手术后第二天就可以下地走动。医生在患儿下肢的血管中放置一根细小的导管,将此导管沿着血管送至心脏,此导管的头端隐藏着房间隔缺损的封堵器,当导管到达心脏缺损处,再通过远程遥控这根导管讲封堵器释放出来而闭合房间隔缺损。(2)外科手术修补缺损。另外一种治疗方式为外科开胸手术,需要体外循环和全麻。手术的方式可以选用正中切口和侧开胸方式,一般选用心包补片来闭合缺损。外科开胸手术相对介入而言手术创伤较大,需要住院10-15天。目前临床上,不适合介入治疗的房间隔缺损和合并有肺静脉畸形的房间隔缺损,选择应用外科开胸手术治疗。6.房间隔缺损可以根治吗?房间隔缺损无论是介入治疗还是外科开胸手术治疗,技术都非常成熟,房间隔缺损闭合后,孩子和正常人一样,可以剧烈运动、结婚生子等等都一切正常。本文系武育蓉医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
武育蓉 主任医师 上海新华医院 儿童心脏中心 小儿心血管科423人已购买 - 患者故事 来自家长的感谢信——新生儿、小婴儿肺动脉瓣狭窄的微创介入治疗
近日,我们心脏中心收到一封来自一位宝爸的感谢信。看着这封长达7页、2471个字的感谢信,我仿佛看到了宝爸的焦虑、希望、忐忑、开心、幸福,我也看到了我们整个医疗团队一直以来不断努力、创新的价值和意义所在。 引用宝爸在感谢信中的一句话“没经历过的人永远不会懂”,作为医患双方,家长能懂我们台前幕后的努力并心怀感激,我们能懂家长的种种不易并心怀敬意。家长感谢我们的救治,我们感谢家长的信任和肯定。 征得宝爸同意,附上感谢信原文:
 彭永宣 主治医师 上海新华医院 小儿心胸外科676人已读
彭永宣 主治医师 上海新华医院 小儿心胸外科676人已读 - 直播回放 胎儿及儿童先心病的诊疗
直播时间:2022年05月31日19:57主讲人:武育蓉主任医师上海交通大学医学院附属新华医院小儿心血管科问题及答案:问题:就是卵圆孔和心肌酶视频解答:点击这里查看详情>>>问题:卵圆孔未必视频解答:点击这里查看详情>>>问题:爱心劵怎么用视频解答:点击这里查看详情>>>问题:这个和心肌酶高没关系吧视频解答:点击这里查看详情>>>问题:体重15斤,介入后并发症有哪些?视频解答:点击这里查看详情>>>问题:宝宝3个月时候卵圆孔未闭1.5mm,严重吗现在8个多月了,现不配合心脏彩超,什么时候做比较好问题:维生素1-5宝宝6.89视频解答:点击这里查看详情>>>问题:是要下载好大夫在线的APP视频解答:点击这里查看详情>>>问题:室间隔肌部室缺介入封堵会影响传导束吗?视频解答:点击这里查看详情>>>问题:9个月大女宝,房缺0.77cm,继发型,近中央部位,适合介入吗视频解答:点击这里查看详情>>>问题:如果胎儿时期胎心监护都在160左右出生后如果心脏没问题心跳快的话正常吗视频解答:点击这里查看详情>>>问题:好的谢谢视频解答:点击这里查看详情>>>问题:主任,请问二叶的宝宝没有狭窄和关闭不全,出生就升主稍扩张的常见吗视频解答:点击这里查看详情>>>问题:10个月时查还是高于指标,查了心脏没事,胎儿时期心跳就偏快,目前这个情况,应该怎么处理,是什么问题呢问题:你好孩子现在两岁7个月的时候抽血时发现ast109.9高,肌酸激酶365,肌酸激酶同工酶29视频解答:点击这里查看详情>>>问题:请问一下,孩子房间隔缺损0.35请问严重吗?没有什么明显症状,就是做彩超发现的视频解答:点击这里查看详情>>>问题:孩子现在四个月,没有明显证症状视频解答:点击这里查看详情>>>问题:好的,谢谢,像孩子这种情况可以打防疫针吗视频解答:点击这里查看详情>>>问题:怎么发给您问题:没有不舒服,是做了心脏彩超视频解答:点击这里查看详情>>>问题:矫正性大动脉转位,房间隔缺埙,肺动脉轻度狭窄,有什么好的治疗方案?这种心脏病可以打预防针吗?视频解答:点击这里查看详情>>>问题:吃辅酶的话可以打疫苗吗问题:现在这样可以打疫苗吗视频解答:点击这里查看详情>>>问题:4岁半,4mm肌部近心尖处室间隔缺损,左心室37mm增大严重吗,目前需要尽快手术吗?采用什么手术方式视频解答:点击这里查看详情>>>问题:之前就是叹气才查心肌酶的,现在感觉很少叹气了问题:还需要用药吗,之前同工酶是8.5,不同医院检测单位不同,吃了1个月辅酶后来复查的,现在还需要吃药吗视频解答:点击这里查看详情>>>问题:刚出生几天的宝宝,哭的时候只有一个眼睛流眼泪是怎么回事问题:刚出生的宝宝,哭的时候只有一个眼睛流眼泪是怎么回事问题:我的宝宝,刚出生几天,哭的时候只有一个眼睛流眼泪是怎么回事视频解答:点击这里查看详情>>>问题:谢谢主任,感谢视频解答:点击这里查看详情>>>问题:小儿房缺8mm如果不治疗,一般会怎么发展?视频解答:点击这里查看详情>>>问题:武医生你好,现在复查宝宝心肌酶谱同工酶62,高敏肌钙蛋白正常了,之前都高的,这个还需要检查吗视频解答:点击这里查看详情>>>问题:谢谢武主任问题:家族没有马凡遗传史,宝宝目前身高体重也都胖胖的视频解答:点击这里查看详情>>>问题:动脉导管这个微创手术是怎么做的,需要住院多久?问题:国产和进口的,是不是进口的比较好?视频解答:点击这里查看详情>>>问题:目前没有症状,这个手术需要多少费用视频解答:点击这里查看详情>>>问题:两周岁孩子,动脉导管未闭合,宽约1.54mm,需要手术吗?视频解答:点击这里查看详情>>>问题:宝宝出生就检测说升主内径稍增宽,主动脉功能性二叶,这个是导致升主稍增宽的原因吗,现在就怕孩子是马凡,问题:武主任,请问五个月宝宝升主动脉内径12.9.体重中高,这个扩张严重吗,是什么引起的视频解答:点击这里查看详情>>>问题:2岁9个月中央型房缺78mm,右心偏大,无异常。何时治疗比较好?谢谢视频解答:点击这里查看详情>>>
 武育蓉 主任医师 上海新华医院 儿童心脏中心 小儿心血管科261人已读
武育蓉 主任医师 上海新华医院 儿童心脏中心 小儿心血管科261人已读 - 先心病的治疗:父母也能提供强大的医学专业上的帮助
手术都有最佳的手术时机,但是如果从现在到最佳手术时机的等待期里,孩子随时可能会发生生命危险,需要爸妈做出选择,是保险型的“不想宝宝发生任何危险,现在就手术”,还是胆大型的“为了最佳的手术时机,我们一定会在家里把宝宝照护好”。在我们中心接受手术治疗的一个宝宝的爸妈给出了他们的选择。这个宝宝叫文文,一出生就住在我们医院新生儿重症监护室,因为他在妈妈肚子里就发现有复杂的先天性心脏病——右心室双出口合并肺动脉下室缺(又叫Taussig-Bing畸形)。手术需要把室间隔缺损修补、主动脉和肺动脉位置互换、冠状动脉重新种植,可以说是先心病手术中最高级别难度的手术之一。我们给文文爸妈两个建议,一个是这次住院期间就接受手术,大概宝宝10天半个月大的时候手术,好处是尽快手术,避免等待期间出现病情波动、严重时危及生命,坏处是虽然年龄小、体重轻不一定会降低手术成功率,但是根据文文的情况,他还是有机会可以长大一些再手术;第二个方案是文文目前心脏的多种畸形互相影响,使得血液循环处于一个微妙的平衡状态,如果能良好的维持这种平衡状态,可以让宝宝到三四个月大时再接受手术。(文文的病例详情可以浏览我们公众号的文章:“孩子的病很重,医生却让等了四个月”)文文的爸爸妈妈决定先让文文出院回家,他们在家里尽量照护好,等到他三四个月大了再来手术。我们给文文爸妈留下了微信,在家里有任何问题都可以随时联系上我们,给予医学专业上的帮助和指导。文文爸爸妈妈在家里备好家用制氧机,监测文文的生命体征和氧饱和度,细心的喂养,仔细的观察和处理时不时出现的一些异常情况。中间有两次来我们医院复查,我们也准备好绿色通道,为他们的氧气袋充满氧气以备返回时使用。就这样,虽然是一路提心吊胆,但文文有惊无险的长到4个月,成功接受了手术,顺利出院。先心宝宝的治疗,父母是非常关键的,虽然他们缺少专业知识,但是在医生的远程帮助和指导下,能为提高宝宝术前的状态、促进宝宝术后的康复等方面提供很大很大的帮助。所以,每个孩子最佳的手术时机,不是千篇一律的,而是个体化的,并且随着孩子的状态可以动态调节的。在等待最佳手术期间,父母应该密切关注孩子的状态,和医生保持密切联系,给予孩子最正确的支持,这样就能让孩子在最佳手术时机时接受手术。
彭永宣 主治医师 上海新华医院 小儿心胸外科1282人已读 - 1.9公斤的室间隔缺损修补术——是医生的胆大妄为、治疗激进还是艺高人胆大的妙手回春?
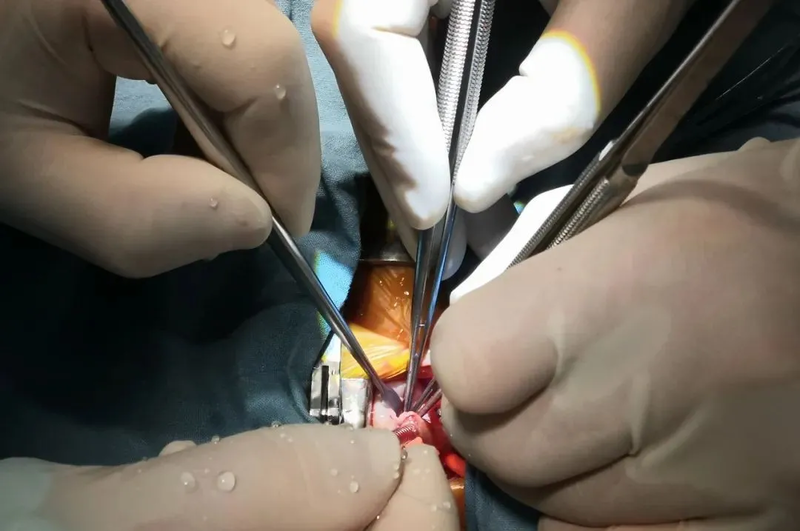
一个还没满月的宝宝,因为提前一个月早产,按照医学上补足预产期,宝宝还是呆在妈妈的肚子里。宝宝的心脏上有1cm大小的室间隔缺损,他的呼吸非常累,吃奶吃不动,所以出生后就一直呆在监护室里。如果不手术,宝宝的心脏和肺很难适应大型室间隔缺损带来的额外负担,而且奶量难以保证,体重没法增长;但是如果手术的话,他的体重只有1.9公斤,他的心脏也就只有30克左右,一个迷你鸡蛋的大小,可能供主刀医生修补室间隔缺损的空间小到只够医生一只眼睛看进去。那到底要怎么办?两难的选择,是胆大、激进,尽快手术!?还是保守、等待,看宝宝造化!?最终,这个宝宝在我们中心成功的完成手术,非常顺利的康复出院,具体治疗经过可以点击链接阅读我们公众号的案例分享(点击链接:新华医院儿童心脏中心:1.9公斤的室间隔缺损手术)。其实室间隔缺损手术的最佳手术时机,还是有一定的规律的:家长须知:任何需要治疗的心脏畸形,即使孩子没有明显临床表现,对孩子的生长发育都是有影响的,换句话说,如果根治了心脏畸形,孩子会生长发育的更加的好。情况1:室间隔缺损小(小于3mm)、自愈可能性高(容易愈合的部位、多次心彩超发现缺损有缩小的趋势)→无明显临床症状(呼吸快、吃奶慢、体重增长慢、容易呼吸道感染)→定期复查(半年到一年的频率);情况2-1:室间隔缺损小(小于3mm)、自愈可能性低(存在主动脉瓣脱垂、肺动脉下、多次复查无缩小的趋势)→无明显临床症状(呼吸快、吃奶慢、体重增长慢、容易呼吸道感染)→定期复查(半年到一年的频率)→学龄前接受外科微创小切口或内科介入封堵手术;情况2-2:室间隔缺损小(小于3mm)、自愈可能性低(存在主动脉瓣脱垂、肺动脉下、多次复查无缩小的趋势)→有明显临床症状(呼吸快、吃奶慢、体重增长慢、容易呼吸道感染)→6月龄后可考虑择期手术;情况3-1:室间隔缺损大(大于5mm)、自愈可能性低(存在主动脉瓣脱垂、肺动脉下、多次复查无缩小的趋势)→无明显临床症状(呼吸快、吃奶慢、体重增长慢、容易呼吸道感染)→早期手术(3月龄后可考虑择期手术);情况3-2:室间隔缺损大(大于5mm)、自愈可能性低(存在主动脉瓣脱垂、肺动脉下、多次复查无缩小的趋势)→有明显临床症状(呼吸快、吃奶慢、体重增长慢、容易呼吸道感染)→尽快手术;情况4:其他情况参照上述情况。
 彭永宣 主治医师 上海新华医院 小儿心胸外科1202人已读
彭永宣 主治医师 上海新华医院 小儿心胸外科1202人已读 - 引用 胎儿先天性心血管疾病产前指导及干预方式的临床选择
随着先天性心血管疾病治疗手段的进步、医学影像技术的发展以及社会经济条件的改善,胎儿心脏病学已成为儿童心脏病学中发展迅速的分支,其所涉疾病包括胎儿心律失常、心血管畸形、心脏肿瘤、心肌疾病、心脏源性及非心脏源性心力衰竭(心衰)等。目前,产前检查能发现绝大部分胎儿先天性心血管疾病并进行准确评估,为产前临床决策及干预提供可靠依据。部分胎儿心律失常、心衰及严重心血管畸形的产前干预探索已获得成功的临床应用,明显改善了患胎预后。在胎儿心脏病学临床实践中,如果缺乏规范的监护、甄别、评估体系,胎儿心血管疾病临床转归及风险评估不明朗等为准父母及临床医生决策带来极大困难,并对选择继续妊娠的孕妇及家庭带来巨大的心理负担;盲目、非选择性终止妊娠会对孕妇及家庭造成极大伤害,不恰当的产前治疗可能置孕妇于不必要的风险之中,违背“母亲安全”这一产前干预的最高原则。由此可见,对胎儿先天性心血管疾病进行甄别随访,对严重病例进行及时恰当的干预,为罹患家庭及准父母提供准确的参考建议及心理辅导,协助做出正确的临床决策,具有极大的社会学及医学意义。胎儿先天性心血管疾病自然史及产前干预临床选择一、胎儿心律失常:胎儿心律失常发生率约1~2%,多数是心脏发育过程中的良性过程,不需特殊干预,预后良好。只有约10%的胎儿心律失常为持续性、会造成胎儿血液动力学明显改变,导致胎儿心衰及水肿,甚至死亡。及时有效的处理往往能控制胎儿心律失常及心衰,并显著减少由于血流动力学改变所导致的胎儿重要脏器继发性损害。因而在妊娠期常规检查中应仔细进行胎心听诊,加强胎儿监护,及早发现问题,尽早明确诊断,及时处理,避免延误诊断处理的最佳时机。具体来讲,①对于出现过心律失常的胎儿定期随访,明确其病情衍变及转归;②对于一过性、非持续性、不会造成胎儿血液动力学改变的胎儿心律失常加强监测,为孕妇及家庭提供正确的咨询、随访指导;③对于随访甄别出来的持续性的、可能会造成或已经造成了胎儿血流动力学明显改变的严重的胎儿心律失常要及时治疗,尽量减少异常血流动力学持续的时间,防止出现胎儿重要脏器损害;④对于终末期的,或经治疗无效甚至加重的胎儿心律失常,及时终止妊娠,确保母亲安全;⑤通过系统研究,探寻出现持续性、可能会造成胎儿血流动力学明显改变的严重的胎儿心律失常的高危或预测因素,指导临床监测。二、胎儿心脏结构异常:绝大多数先天性心血管畸形并不妨碍胎儿的宫内生长发育,出生前后应根据具体情况制定出产后干预策略。对于单纯型先天性心血管畸形及部分复合畸形患胎,出生后心脏外科手术及经导管介入治疗技术成熟,治疗后患者的生活质量及寿命不会受到明显影响。应当注意到,室间隔缺损(VSD)等简单畸形在宫内有自然闭合趋势,但部分单纯畸形在宫内也可能会持续进展,异常的血液动力学状态会引起胎儿心脏腔室及血管发育逐渐迟滞,形成严重心血管畸形,甚至伴发心衰、心律失常,如大型VSD或主动脉瓣狭窄(AS)会导致流经升主动脉、主动脉弓血流减少,出现主动脉弓发育不良、主动脉缩窄等,因而对胎儿期发现的简单心血管畸形应加强随访,出现畸形进展则纳入复杂畸形范畴考虑。按我国卫生部要求,怀孕18-24周必须检出的严重心血管畸形为单腔心,这类患胎可能伴发严重的心衰及心律失常,可能带来孕期严重的母胎并发症。即使患胎能够存活至新生儿期,产后早期死亡率极高,幸存者无建立双心室循环的可能,进一步分期姑息手术疗效差,术后严重并发症率高,生存质量极差,一经发现,建议终止妊娠。对于部分严重心血管畸形,如严重 AS和/或限制性房间通道(R-IAC)引起的左心发育不良综合征、伴R-IAC的室间隔完整型肺动脉闭锁等,多数病例在出生前业已发生心脏腔室及体、肺血管床不可逆病变,甚至出现胎儿水肿、死亡,失去进一步治疗机会。目前国外多个医学中心对这一部分病例尝试实施妊娠中后期胎儿心脏主/肺动脉球囊成形术,希望形成趋于正常的血液动力学状态,促进胎儿心脏腔室重新发育,重塑体/肺血管床,使出生后有机会进一步姑息治疗或建立双心室循环,改善患胎预后。在我们的临床工作中,对这一部分病人应加强监护,动态随访,对没有治疗前途者及时终止妊娠。对于其他复杂心血管畸形,如法洛四联症、右室双出口、心内膜垫缺损、完全性大动脉转位等,因为胎儿循环的特殊性,孕期这些畸形异常的血液动力学对胎儿心脏腔室及体肺血管床无明显影响。但出生后胎儿循环向成人循环转换,畸形所带来的症状就会逐渐显现,部分患者需要出生后急诊姑息或根治手术。因此发现这类畸形后,应密切监测其心脏功能、心搏节律及心脏腔室大小动态发育情况,建议孕妇在有条件的医学中心分娩,以便新生儿出生后能够得到最有效的救治。三、胎儿心脏肿瘤及心肌疾病:1、胎儿心脏肿瘤:原发性心脏肿瘤可发生于心腔、心内膜、心肌、心外膜或各种情况合并存在,心脏肿瘤十分罕见,发病率约为0.02%左右,胎儿期报道更为少见。尽管胎儿心脏肿瘤的自然史尚未清楚,但早期的产前诊断对于恰当的产前处理及孕期胎儿监护都非常重要。胎儿期最常发生的良性心脏肿瘤是横纹肌瘤、纤维瘤、畸胎瘤及粘液瘤等。小型心脏良性肿瘤可无症状, 大型肿瘤由于肿瘤阻塞房室瓣口可引起血流动力学障碍。累及心脏传导系统的心脏肿瘤会导致心律失常。胎儿良性心脏肿瘤的预后决定于是否有并发症,如心律失常或者流出道梗阻,出现胎儿水肿则是致死性并发症。胎儿期发现的心脏良性肿瘤病例,应加强随访,了解肿瘤生长状态、胎儿血液动力学状态、有无心律失常及心力衰竭等协助临床判断。原发性心脏恶性肿瘤是较少见的肿瘤, 发病率为0.002%~0. 003%,胎儿期原发性心脏恶性肿瘤偶见报道,多为肉瘤类。此外还有转移性肿瘤(继发于胎儿期神经母细胞瘤、白血病等),肿瘤可迅速侵及心脏各层结构,并侵入邻近纵隔器官和广泛转移,心衰、栓塞、心包积液、心包填塞及心律失常,预后差,胎儿期患者多早期死亡。2、胎儿心肌疾病:胎儿心肌疾病发生率低,扩张性及限制性心肌病均仅有零星报道。患糖尿病孕妇的胎儿暴露于高血糖环境中,孕早期可影响心脏发育产生畸形,在孕晚期可引发特殊类型的肥厚型心肌病,同时影响胎儿心脏的结构和功能。胎儿暴露于维拉帕米会导致肥厚性心肌病发生率增加。在患免疫性疾病孕妇(如红斑狼疮)中,孕妇抗-SSA和/或抗-SSB等抗体通过胎盘运输到达胎儿循环引起胎儿心肌损害,各型心肌病(扩张型心肌病为主)及胎儿先天性房室传导阻滞(AVB)发病率增加。有研究表明孕妇血浆IL-1/IL-1ra比值改变以及IL-1及其拮抗剂的失调可以促成胎儿心血管功能的平衡紊乱,从而导致心肌疾病的发生。胎儿期发病的家族性心肌致密化不全或线粒体、细胞支架、Z线、以及肌节蛋白变异等导致的心肌致密化不全可表现为严重的胎儿水肿。此外,胎儿长时间的心动过速也可导致心肌病。胎儿期发生的心肌病进展快,预后差,多数迅速出现胎儿心衰、死胎。四、胎儿心力衰竭:分为心脏源性及非心脏源性胎儿心脏源性心衰的常见原因有异常外周血管阻抗引起血流重新分配、贫血或动静脉瘘致高心排血量、原发或继发性瓣膜返流、心肌病变及功能不良、心动过速/过缓、心脏肿瘤等。胎儿非心脏源性心衰的常见原因有免疫性胎儿水肿、胎儿先天性膈疝、骶尾部畸胎瘤等其他器官系统畸形所致的心衰、遗传代谢性疾病累及心脏导致的心衰以及一些未明的原因。在处理宫内心脏源性及非心脏源性胎儿心衰时,需对原发病同时进行处理。心衰的处理以有效提高心排血量为目的,达到延长孕期、防止早产和围产期窒息,对严重、无生存希望的病例可及时终止妊娠。胎儿先天性心血管疾病产前干预方法及展望一、产前干预伦理学原则:现代医学伦理学认为,对某种预后极差的、可能导致胎儿、新生儿及儿童死亡的出生缺陷进行产前干预改善预后是合乎伦理学基本准则的。胎儿先天性心血管畸形产前干预的伦理学原则:①该类先天性心血管畸形生后治疗效果差,死亡率高;②拟施行的干预措施可行,并能够纠正心脏畸形,或逆转、阻止、延缓畸形发展,改善生后治疗效果;③胎儿心血管畸形尚未进展到经宫内干预也无法有效恢复的程度;④必须将孕母的安全、健康放在首要位置,还必须考虑到孕母未来的生育能力。二、产前干预方法:即胎儿心脏介入治疗(FCI)1、药物性FCI:主要指胎儿快速性、缓慢性心律失常及胎儿心衰药物治疗。目前经孕母口服药物经胎盘治疗胎儿疾病是首选治疗途径。因脐静脉穿刺可能导致胎儿心动过缓等并发症,可能会加重胎儿心律失常及心衰,因而仅在严重水肿胎盘转运率极低时才考虑使用。快速性胎儿心律失常药物FCI方面,研究主要集中在孕母口服地高辛和/或索他洛尔治疗胎儿室上性心动过速和胎儿心房扑动,转复率可达50-83%。治疗后最理想状态是转复为窦性心律,最低限度是控制心室率,保证胎儿联合心输出量及重要脏器灌注,减少继发性损伤。有研究报道经脐静脉穿刺成功后,经脐血管注射ATP或胺碘酮治疗胎儿SVT取得良好疗效,并推荐经脐血管注射胺碘酮可用于药物抵抗性胎儿快速性心律失常。胎儿缓慢性心律失常药物FCI主要包括拟交感肾上腺素、地塞米松等药物单用或联合治疗胎儿AVB、窦性心动过缓,通常能做到提高心室率,满足胎儿生长发育所需。多中心研究发现,地塞米松不能逆转高度AVB,但能阻止免疫性胎儿Ⅰ度AVB发展为Ⅱ、Ⅲ度AVB,因而对孕母患有免疫性疾病胎儿发生的Ⅰ度AVB应及早治疗,防止疾病进展。胎儿心衰药物FCI主要采用孕母口服地高辛经胎盘转运治疗,并同时针对原发病进行治疗,疗程取决于原发性疾病种类。2、开放性FCI:指经子宫创口直径≥3mm的外科手术,包括胎儿镜手术。在体外循环及直视下行胎儿心脏外科手术,解剖纠治心脏畸形,使胎儿心脏腔室和体/肺血管床正常发育,从理论上讲是胎儿严重心血管畸形产前干预最理想的方式。但胎儿体外循环导致胎盘功能不良及子宫切开带来的不可避免的、影响妊娠结局的早产等因素限制了开放性FCI的临床运用。3、闭合性FCI:即狭义的胎儿心脏介入手术,指器械通过子宫穿刺孔直径<3mm的胎儿心脏介入手术。闭合性FCI无须子宫切开及胎儿体外循环,避免了胎儿外置,是极具发展潜力的严重心血管畸形产前干预方式。闭合性FCI可在一定程度上改变畸形心脏的病理生理状态,允许心脏腔室及体肺血管床有效生长发育,使之具有出生后治疗的机会,并提高新生儿的手术耐受力。闭合性FCI目前主要包括超声引导下经皮或经子宫穿刺的宫内主/肺动脉瓣球囊成形术、球囊房隔造口术等。目前这一领域研究中最卓有成效的是Boston儿童医院。2000年至今,该院已进行了120例胎儿心脏介入手术,其中88例胎儿主动脉瓣球囊成形术、11例胎儿肺动脉瓣球囊成形术及21例胎儿球囊房隔造口术,无孕母并发症发生,技术成功率达75~80%。该组资料中,实施宫内主动脉瓣球囊成形术的患胎出生后,30%一期手术建立了双室循环,8%在一期姑息后二期手术建立双室循环,其余患胎/儿的主动脉瓣、二尖瓣及左心室较对照组也有不同程度发育;施行宫内球囊房隔造口术后,≥3mm的房隔通道能明显提高患胎出生后的氧饱和度,降低急诊外科左房减压的风险;胚胎期右室发育早于左室,因而肺动脉瓣球囊成形术能在孕中期顺利实施,历经宫内肺动脉瓣球囊成形术的患胎有充足的术后宫内恢复时间,因而出生后均能建立双心室循环。临床结果表明,适时的FCI能明显改善患胎预后,最终临床疗效与FCI实施时间选择密切相关。三、胎儿心血管疾病产前干预的展望:经过多年的基础及临床研究,各国学者在胎儿期心血管疾病产前干预方面积累了一定的经验。但还需对产前干预的患者筛选、实施时机及综合治疗方案等进行系统研究。如果胎儿心血管疾病已经发展到经宫内干预也无法有效恢复的程度,产前干预或许是无益的,甚至是有风险的;如果术后没有充足的宫内恢复时间,产前干预的效益就不能得到充分发挥。因此,制定患胎纳入/排除标准,把握恰当的产前干预时机,深入研究预后影响因素非常必要。国外多家心脏中心正在进行胎儿心脏介入手术的“患者筛选” 研究,选择“恰当的”或“有价值的”患胎进行产前干预,实现产前干预效益最大化。希望通过相关研究能够建立有效的宫内产前干预患者筛选标准,对适宜病例给予恰当的产前干预方案,使产前干预真正成为利大于弊的、有用的临床工具。
华益民 主任医师 四川大学华西第二医院 儿童心血管科6489人已读 - 引用 胎儿心力衰竭的准确评估及治疗
胎儿期心脏发育监测包括对胎儿心脏及其整体功能状态进行准确诊断、生理评价、有效治疗、结局预测(妊娠结局、新生儿结局、短期及长期结局)等,综合起来就是要对胎儿心血管系统疾病进行准确诊断和有效治疗,这有赖于胎儿心脏病学研究诸多方面的最新进展,特别是治疗方法的进步,在胎儿心力衰竭的诊断、评估及治疗等方面尤为如此[1-2]。 胎儿心力衰竭的常见原因有胎儿心律失常、贫血、先天性心脏病伴瓣膜返流、心外畸形(如先天性隔疝、畸胎瘤等)、胎儿系统性感染、胎胎输血受血者血容量及血压超负荷、房室瘘伴高心排等等[1-2]。导致胎儿水肿的机理可多种并存,使其原发病因被掩盖。围产期心脏科医师可从以下几个方面对胎儿水肿进行评估:胎儿水肿是心源性的么?胎儿心力衰竭是否为先天性心脏病所导致?是稳定性或进展型胎儿水肿/心力衰竭?胎儿心力衰竭的持续时间及严重程度如何?有无胎儿心肌功能不良发生?胎儿心力衰竭的长期预后判断依赖于脏器灌注不良状态的时间、程度,以及是否发生了不可逆脏器损伤,尤其是脑损伤。一、胎儿心力衰竭的准确诊断、评估及预后判断 胎儿心力衰竭的临床表现为胎儿心脏扩大、胎儿水肿以及瓣膜反流出现或加重。针对性的胎儿超声心动图须采集到胎儿心胸面积比(cardiac / thoracic area ratio, C:T)、静脉血流频谱(下腔静脉、肝静脉、脐静脉)、四组瓣膜血流频谱、胎儿水肿发生部位及程度等信息以提供临床判断[1-2]。 目前,胎儿心血管功能的评价指标主要有心血管整体评分(cardiovascular profile score,CVPS)、心脏作功指数(Tei-指数)、脐动脉阻力指数(umbilical artery resistance index, UARI)、搏动指数(pulsatility index, PI)以及收缩期最高血流速度S与舒张期最低血流速度D的比值(S/D)。1、CVPS:CVPS是较为完善的胎儿心力衰竭半定量评价指标,由胎儿水肿、心/ 胸面积比值、心脏功能、脐静脉和静脉导管血流频谱以及脐动脉血流频谱组成,每个项目2分,总分10分,分述如下[1-8]: 胎儿水肿:严重心力衰竭可引起胎儿水肿。早期表现为腹腔、胸膜腔和心包腔积液或多浆膜腔积液(CVPS评分减1分),水肿加重时表现为皮肤水肿(CVPS评分减2分)。胎儿水肿的围产期死亡率高达72%,伴有心脏或心外畸形者死亡率更高达80%~100%。 胎儿心脏扩大:正常胎儿心/ 胸面积比值为0.20~0.35之间。心脏扩大定义为在妊娠各期二维超声心动图检测心/ 胸面积比值大于0.35。当这一比值<0.20或>0.50则患胎预后更差。 心脏功能:主要包括房室瓣返流及入室血流频谱情况,正常胎儿房室瓣完整且活动度好,出现全收缩期三尖瓣反流则CVPS评分减1分,出现全收缩期二尖瓣反流或入室血流频谱为单相性充盈,CVPS评分减2分。正常胎儿可存在微量收缩早期三尖瓣反流,但如果其持续时限大于70ms则预示异常,需要进一步检查。在明显三尖瓣返流基础上出现二尖瓣反流提示严重心力衰竭,合并其他瓣膜返流则是胎心充血性心力衰竭进展的表现。正常胎儿入室血流频谱为双相性充盈,先是心室舒张主动抽吸所产生的较小的E 峰,紧随其后是心房收缩射血入心室产生的较大的A峰,随着孕龄增加,心肌顺应性逐渐提高,E峰逐渐增大,A峰逐渐缩小,至出生后及成人均为E峰>A峰,E峰消失则入室血流频谱呈现单一波形,即单相性充盈频谱,提示心脏舒张功能严重受损,伴有严重心力衰竭和不良预后。 静脉血流频谱:正常情况下,胎儿脐静脉血流是非搏动性的,静脉导管血流呈低搏动性。静脉导管血流为胎儿静脉系统最快的血流,为双期连续血流。心房压增加可导致静脉血流搏动性增强,血流速度减慢。如果前向血流速度为零或出现反向血流,CVPS评分减1分,出现脐静脉搏动则CVPS评分减2分。心力衰竭终末期表现是房性脐静脉搏动,即所谓“舒张阻滞”或“双静脉搏动”(脐静脉和下腔静脉血流频谱相同),是预示胎儿可能发生围产期死亡的紧急征象。 动脉血流频谱:在正常胎儿脐动脉可检测到全收缩期正向血流。如缺乏舒张末血流则CVPS评分减1分,如舒张末出现反向血流则CVPS评分减2分,提示预后不良。2、Tei指数: Tei指数是评价胎儿心功能的实用指标,具有很多优点,诸如不受心室几何形状以及心率影响,在胎儿期不受孕周影响,测量方法简便,重复性强等。研究证明Tei指数能够可靠评价水肿胎儿的心脏功能[9-10],随着孕龄增加,Tei指数下降代表心肌的发育和成熟。但孕早期心脏体积小,胎儿心室Tei指数的检测较困难;对心律失常患胎Tei指数的应用受到限制[9]。Tei 指数的潜在应用价值尚有待进一步研究。3、UARI、PI、S/D S/D、RI、PI主要反映血管床的阻力状态,通过多普勒波形分析,间接获知血液动力学状况[11-12]。通过动脉的血流波型,计算公式:S/D= PSV/ EDV,RI=PSV×EDV/PSV,PI=(PSV-EDV)/ Vm,其中PSV为收缩期血流峰速,EDV为舒张末期血流速度,Vm为平均血流速度。上述三个参数可作为反映动脉某一横断面的顺应性和血流弹性阻力的指标,对脏器实质损害及血液动力学变化程度进行客观的、定量的评价,脏器实质损伤时由于末梢血管阻力增加或血液动力学显著变化时末梢血管充盈减少,舒张期血流减少,使RI 、PI及S/D增大。S/D比值、RI、PI的含义完全一致,可以相互替代,临床上多用S/D比值作为观测脐动脉血流的指标。一般认为,随着妊娠进展,胎儿胎盘循环阻力降低,脐带舒张期的血流稳定增长,胎儿脐动脉S/D值降低,有助于胎儿的发育,妊娠期S/D≥3.0是危险信号,应进行密切监测,而S/D≤2.5则被认为胎儿是安全的。 从CVPS的5个检测项目可以看出其所涉及的症状体征多在心力衰竭中后期出现,所以孕早期CVPS 测量能否早期预测胎儿结局还需进一步研究。有报道认为,CVPS和Tei指数呈负相关关系,而Tei指数异常和水肿胎儿疾病严重性是相关的[13],Tei指数与脐动脉S/D成正相关关系,S/D及Tei指数变化较CVPS更为敏感[14]。因而在胎儿心力衰竭临床实践中,联合多指标进行病情评估、治疗指导、动态监测对心力衰竭胎儿的诊断治疗必将更加具有指导意义。二、胎儿心力衰竭的治疗[14-28] 胎儿心力衰竭药物治疗的目的不仅是要提高有效心输出量,而且应当注重延长孕期、预防早产及围产期缺血缺氧发生。目前关于胎儿药代动力学研究尚少,在胎儿水肿、低蛋白血症等病理状态下药物分布容积、半衰期等可能有很大变化,迄今尚无有关胎儿药物稳态动力学理论及实验的系统研究,因而仅能参照出生后人群的药代动力学和药效学特点进行药物选择。在特定病例开始治疗前应有明确治疗方案,尽可能选用治疗窗较宽的药物,并尽量选用FDA-A类药物(孕妇及胎儿随机对照试验显示无母胎风险),次选FDA-B类、C类药物(B类:动物试验未显示对胎儿的危险,但无孕妇对照组,或对动物生殖试验显示有副反应,但早孕妇女对照组中不能肯定其副反应,C类:动物实验中证实对胎儿有副反应,但在妇女中无对照组或在妇女和动物研究中无相关资料,仅在权衡对胎儿利大于弊时给予该药物),不能使用FDA-D类、X类药物(D类:对人类胎儿有风险的证据,使用时需权衡利弊,X类:孕妇禁忌)。 地高辛属FDA-C类药物,但只要能密切监测并控制母胎血药浓度,绝大部分情况下都能实现利大于弊,且具有确切疗效,因而地高辛目前仍然为胎儿心力衰竭的一线治疗药物。其给药方式主要采用经胎盘转运进行,经脐静脉或胎儿心腔的给药方式可能导致胎儿心动过缓、心包积血等会加重心力衰竭,因而仅在严重水肿胎盘转运率极低时方才考虑使用。文献中地高辛治疗胎儿心力衰竭的推荐剂量为母亲口服地高辛负荷量0.375~0.5mg/次,1~2次后给予维持量0.25 mg/次,每天2~4次,根据母亲血药浓度调整服药次数,一般能迅速保持母亲血药浓度在1.0~2.0ng/ml,在无胎盘水肿等情况下,母胎地高辛经胎盘转运率为75~80%,因而上述推荐剂量能够保证母胎血药浓度比且避免了对母亲的毒副作用。遗传药理学研究表明,不同人种间在药物生物转化及排泄等体内过程上存在着差异,药物敏感性也有差别,因而中国妊娠妇女地高辛剂量低于国外文献报道中的剂量,推荐为负荷量0.25mg/次,8小时1次,2剂后改为维持量0.125~0.25mg/次,每天2次,并进行地高辛血药浓度的动态监测及药物调整。 对于不同原因引起的胎儿心力衰竭,必须针对原发病进行治疗,地高辛仅能作为辅助治疗措施、或原发病解除后对胎儿心功能的支持治疗。比如快速性胎儿心律失常引起的胎儿水肿,因为地高辛的抗快速性心律失常作用,因而可以单用地高辛同时治疗心律失常及心力衰竭,也可考虑单用或联用索他洛尔(FDA-B类)、腺苷(FDA-C类)、氟尼卡(FDA-C类)、胺碘酮(FDA-D类)等药物进行;胎儿系统感染引起的水肿,应当进行针对感染病原的治疗;胎儿贫血性水肿可以进行胎儿输血治疗;胎儿缓慢性心律失常导致的水肿则应当进行提升心室率及抑制免疫损伤等治疗;通过宫内主/肺动脉瓣球囊成形术治疗宫内严重主动脉瓣狭窄、肺动脉瓣狭窄引起的胎儿水肿;通过胎儿镜手术治疗先天性隔疝、畸胎瘤等,从而治疗这些心外畸形导致的胎儿心力衰竭等。 胎儿心力衰竭的诊断并不困难,但要判定这些异常变化的瞬变性或持久性、要明确其原发病因及机制、要准确把握其持续时间及严重程度、要对疾病个体制定恰当的治疗方案及进行准确的预后判断,在胎儿心脏病学研究领域中,上述问题都是儿科、心血管科及产科医师所面临的极大挑战。参考文献:[1] Huhta J.C. Guideline for evaluation of heart failure in the fetus with or without hydrops. Pediatr cardiol. 2004, 25: 274-286[2] Ojala TH, Hornberger LK, Fetal heart failure. Front Biosci (Schol Ed).891-906 P20515832[3]Cornelia H, Manfred H, Sturlia H, et al. A cardiovascular profile score in the surveillance of fetal hydrops. The Journal of Maternal-Fetal and Neonatal Medicine, 2006, 19(7):407-413[4] Huhta JC .Fetal congestive heart failure. Seminars in Fetal &Neonatal Medicine . 2005, 10: 542-552[5] Berg C, Kermer C, Geipel A, et al. Ductus venosus blood alterations in fetuses with obstructive lesion of the right heart. Ultrosound Obstet Gynecol.2006, 28:137-142[6] Hofstaetter C, Gudmundsson S. Venous Doppler in the evaluation of fetal hydrops. Obstet Gynecol Int. 2010, 2010(1):430157[7] Baschat AA. Ductus venosus Doppler for fetal surveillance in high-risk pregnancies. Clin Obstet Gynecol. 2010, 53(4):858-868[8] Tutschek B, Schmidt KG. Techniques for assessing cardiac output and fetal cardiac function. Semin Fetal Neonatal Med. 2011,16(1):13-21[9]Bruch C , Schmermund A , Marin D , et al. Tei index in patients with mild-to-moderate congestive failure. Eur Heart J, 2000, 21: 1888-1895.[10]Misumi I, Harada E, Doi H, et al. Tei index evaluated by M-mode echocardiography in patients with dilated cardiomyopathy. J Cardiol, 2002, 39:85-91.[11]Ebrashy A, Azmy O, Ibrahim M, et al. Middle cerebral/umbilical artery resistance index ratio as sensitive parameter for fetal well-being and neonatal outcome in patients with preeclampsia: case-control study. Croat Med J. 2005, 46(5):821-825[12]Tan AE, Norizah WM, Rahman HA, et al. Umbilical artery resistance index in diabetic pregnancies: the associations with fetal outcome and neonatal septal hypertrophic cardiomyopathy; J Obstet Gynaecol Res.2005, 31(4):296-301[13]Falkensammer F, James P, Huhta JC. Fetal congestive heart failure : correlation of Tei-index and Cardiovascular-score. J Perinat Med , 2001, 29 :390-398[14] Zhou KY, Hua YM, Zhu Q, et al. Transplacental Digoxin Therapy for Fetal Tachyarrhythmia with Multiple Evaluation Systems. The Journal of Maternal-Fetal & Neonatal Medicine. 2011 (In press)[15] Sbragia L; Intrauterine fetal abnormalities therapy. Rev Bras Ginecol Obstet.:47-54 P20209262[16] Hahurij ND, Blom NA, Lopriore E, Aziz MI, Nagel HT, Rozendaal L, Vandenbussche FP. Perinatal management and long-term cardiac outcome in fetal arrhythmia. Early Hum Dev.:83-87 P21109370[17] Lopriore E, Aziz MI, Nagel HT, et al. Long-term neurodevelopmental outcome after fetal arrhythmia [J]. Am J Obstet Gynecol, 2009, 2001(1): 46. e1-5.[18] Patel D, Cuneo B, Viesca R, et al. Digoxin for the treatment of fetal congestive heart failure with sinus rhythm assessed by cardiovascular profile score [J]. J Matern Fetal Neonatal Med, 2008, 21(7): 477-482.[19] Al-Buhtori M, Moore L, Benbow EW, Cooper RJ. Viral detection in hydrops fetalis, spontaneous abortion, and unexplained fetal death in utero. J Med Virol. 2011,83(4):679-84[20] Enders M, Klingel K, Weidner A, Baisch C, Kandolf R, Schalasta G, Enders G. Risk of fetal hydrops and non-hydropic late intrauterine fetal death after gestational parvovirus B19 infection. J Clin Virol.:163-8 P20729141[21] Ryuji K, Azusa F, Takako K, Jun M, Machiko N, Yuri T, et al. Changes in digoxin pharmacokinetics treated with lipopolysaccharide in Wistar rats.Biol Pharm Bull.2008,31(6)1221-1225[22]Matthew Dawes. Drugs in pregnancy. Pharmacokinetics in pregnancy.Best Pract ResClin Obstet Gynaecol.2001,15(6):819-826[23]Tworetzky W, McElhinney DB, Marx GR, Benson CB, Brusseau R, Morash D, Louise E, Wilkins-Haug LE, Lock JE, Marshall AC. In utero valvuloplasty for pulmonary valve atresia with hypoplastic right ventricle: techniques and outcomes. Pediatrics. 2009 Aug 24.[24]McElhinney DB, Marshall AC, Wilkins-Haug LE, Brown DW, Benson CB, Silva V, Marx GR, Mizrahi-Arnaud A, Lock JE, Tworetzky W. Predictors of technical success and postnatal biventricular outcome after in utero aortic valvuloplasty for aortic stenosis with evolving hypoplastic left heart syndrome. Circulation. 2009; 120:1482–1490.[25]T. Kohl, R. Hering, P. Van de Vondel, et al. Analysis of the stepwise clinical introduction of experimental percutaneous fetoscopic surgical techniques for upcoming minimally invasive fetal cardiac interventions. Surg Endosc 2006, 20(11): 1134-1143[26]Schmolling J, Renke K, Richter O, et al. Digoxin, flecainide, and amiodarone transfer across the placenta and the effects of an elevated umbilical venous pressure on the transfer rate [J]. Ther Drug Monit, 2000, 22(5): 582-588.[27]Schleich JM, Bernard Du Haut Cilly F, Laurent MC, et al. Early prenatal management of a fetal ventricular tachycardia treated in utero by amiodarone with long term follow-up [J]. Prenat Diagn, 2000, 20(6): 449-452.[28]Mevorach D, Elchalal U, Rein AJ. Prevention of complete heart block in children of mothers with anti-SSA/Ro and anti-SSB/La autoantibodies: Detection and treatment of first-degree atrioventricular block [J]. Curr Opin Rheumatol, 2009, 21(5): 478-482.
华益民 主任医师 四川大学华西第二医院 儿童心血管科1.1万人已读 - 引用 胎儿期发现右位主动脉弓,对孩子会有什么影响?
如果胎儿排畸超声,或胎儿心脏超声检查中发现了“右位主动脉弓”,常会使准爸妈很紧张,不知道这会对孩子将来有什么影响。下面就具体谈一谈。正常情况下,主动脉弓在气管和食管的左侧。右位主动脉弓是一种比较常见的解剖变异,顾名思义就是主动脉弓位于气管和食管的右侧。这种情况下主动脉弓会向后、向左延伸,与位于脊柱左侧的降主动脉相连。右位主动脉弓部发出的几支头臂血管(如无名动脉、颈动脉、锁骨下动脉等)的分支方向,与正常左位主动脉弓的分支方向呈镜面关系。右位主动脉弓时,如果由降主动脉发出了左位动脉导管(动脉导管出生后关闭,成为动脉韧带)(下左图所示),或左锁骨下动脉(即迷走左锁骨下动脉)(下右图所示),这两支血管会在食管、气管后向左走形,这样就与右位主动脉弓在空间上形成了一个包绕着气管和食管的环形血管结构,这就是临床上所说的“血管环”的一种。血管环有可能会使气管和食管受压迫,致使孩子出生后出现呼吸困难、喘鸣和反复呼吸道感染,吞咽困难、进食缓慢和生长发育落后等症状。胎儿期超声发现右位主动脉弓的另一个提示是,胎儿“有可能”合并心脏畸形、心脏以外的其他器官畸形及染色体异常。因此,如果排畸超声发现右位主动脉弓,则有必要做一个专门的胎儿心脏超声,仔细观察心脏结构,除外先天性心脏病。但如果没有其他心脏畸形,也没有心脏外畸形,这种孤立性的右位主动脉弓,合并染色体异常的风险通常很低。曾有研究统计约12%的右位主动脉弓会出现气管、食管受压症状,但临床观察并没有这么高的发生率。例如,约30-40%的法洛四联症、肺动脉闭锁约合并右位主动脉弓,但却很少有患儿出现气管、食管压迫症状需要治疗。原因在于右位主动脉弓、左位动脉导管和迷走左锁骨下动脉构成的血管环,空间上较为宽松,绝大多数病例不会压迫气管和食管,也就无需处置。少数有压迫症状的,与其他类型的血管环,如双弓畸形、肺动脉吊带等相比,症状出现相对较晚,多在1岁后出现;也相对较轻。部分病例随着孩子生长,症状还可减轻或缓解。但若在孩子出生后6个月内即出现压迫症状者,提示病情往往会较重,需要积极治疗。治疗方式是外科手术切除动脉导管或动脉韧带。迷走左锁骨下动脉一般无需处置。但若其根部存在瘤样扩张,则有发生重度气管食管压迫的风险,需要一并处理。手术效果总体比较好。
凌雁 副主任医师 北京安贞医院 小儿心脏中心内科130人已购买







